小鼠基因编辑神器

想知道如何在小鼠基因组中实现小到 1 个碱基对的改变,大到上百 Mb 的编辑?
我们到底是怎么做到指哪打哪的精确基因修饰的呢?
今天我们的话题就是小鼠基因组定点编辑技术。
工欲善其事,必先利其器。我们手里可真是有两把刷子的!
● ES 细胞打靶技术
● CRISPR/Cas9 技术
让我们一一道来,前方高能干货预警!
ES 细胞打靶
在小鼠胚胎干细胞(ES 细胞)中进行 DNA 同源重组,将 ES 细胞重新注射到囊胚腔中,可以形成嵌合胚胎,并能在假孕小鼠体内发育,最终发育为嵌合体小鼠。这种嵌合小鼠的组织细胞(包括生殖细胞)可以分别来自囊胚的细胞和被注射的 ES 细胞。因此,通过嵌合小鼠和野生型小鼠的交配,ES 细胞中的遗传信息就能够传递到后代的小鼠个体中。
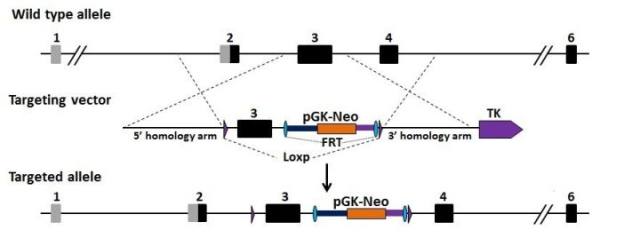
图 1. ES 细胞打靶载体基本结构及原理(图片来自内部资料)
利用 ES 细胞打靶技术建立基因修饰小鼠模型的主要技术路线:
(1)构建重组基因载体(正负双向选择系统);
(2)用电穿孔等方法把重组 DNA 转入受体 ES 细胞内;
(3)用选择培养基筛选抗药 ES 细胞,并利用 PCR 或或 Southern blot 等方法鉴定发生正确同源重组的 ES 细胞;
(4)将中靶 ES 细胞注射到受体囊胚中,将注射后存活的胚胎移植到假孕小鼠子宫中,让其受孕,待小鼠出生后,通过观察毛色的嵌合与否和嵌合程度判断是否获得嵌合体小鼠。
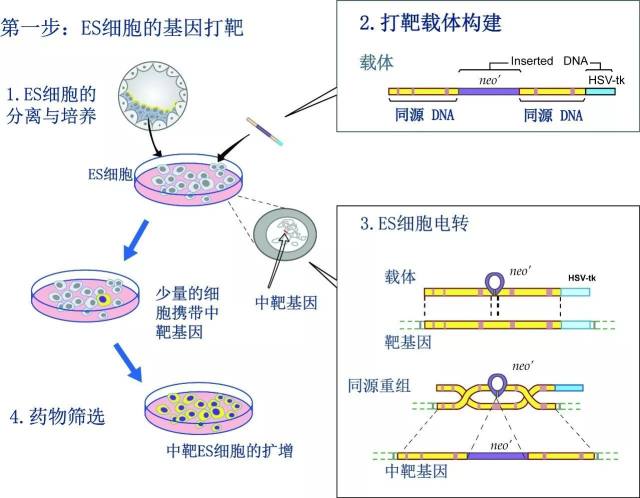
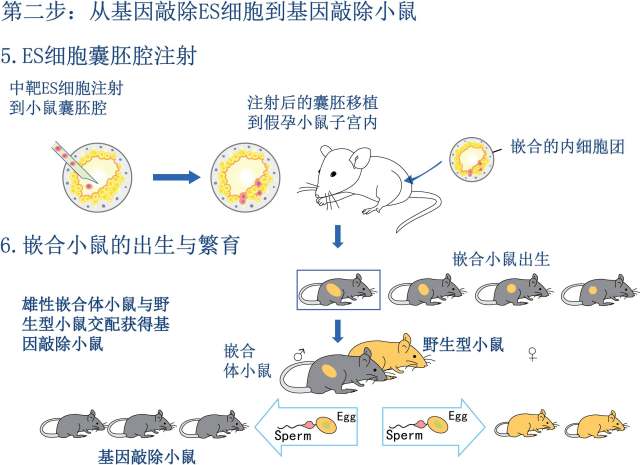
图 2. ES 细胞打靶技术路线(图片来自内部资料)
CRISPR/Cas9 技术
CRISPR/Cas 是细菌和古细菌在长期演化过程中形成的一种高度保守的适应性免疫防御系统,可用来对抗入侵的病毒及外源 DNA。
CRISPR 是 Clustered regularly interspaced short palindromic repeats(规律成簇间隔短回文重复)的缩写。CRISPR 簇是一个广泛存在于细菌和古生菌基因组中的特殊 DNA 重复序列家族,其序列由一个前导区 (Leader)、多个短而高度保守的重复序列区 (Repeat) 和多个间隔区 (Spacer) 组成。
Cas 则是在 CRISPR 附近的一个多态性家族基因,这个家族基因编码的蛋白均含有可与核酸发生作用的功能域,并且与 CRISPR 区域共同发挥作用,因此被命名为 CRISPR 关联基因 (CRISPR associated),缩写为 Cas,包括 Cas1~Cas10 等多种类型。
当细菌抵御噬菌体等外源 DNA 入侵时,在前导区的调控下,CRISPR 被转录成 pre-crRNA,然后被加工成一系列短的含有保守重复序列和间隔区的成熟 crRNA,最终识别并结合到与其互补的外源 DNA 序列上发挥剪切作用。
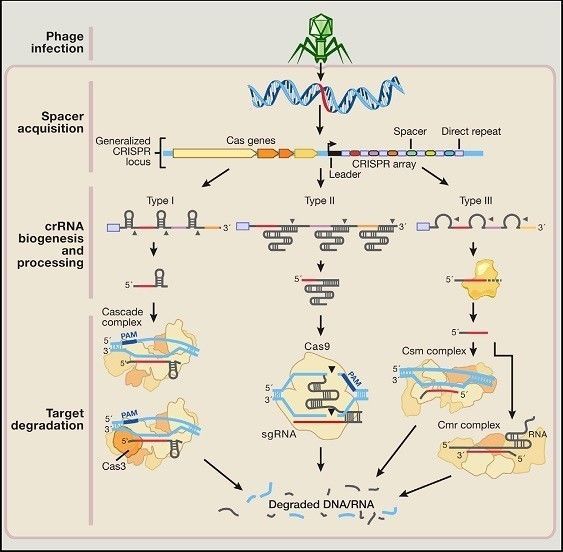
图 3. 细菌 CRISPR/Cas 系统抵御外来入侵原理示意图(图片来自 Cell. 2014 Jun 5;157(6):1262-78.)
目前在基因编辑应用最为广泛的 CRISPR/Cas9 系统是以 Cas9 蛋白以及向导 RNA(gRNA)为核心组成。Cas9 含有在氨基末端的 RuvC 和蛋白质中部的 HNH 两个活性位点,在 crRNA 成熟和双链 DNA 剪切中发挥作用,引起 DNA 双链断裂。CRISPR/Cas9 的剪切位点位于 crRNA 互补序列下游邻近的 PAM 区(Protospacer Adjacent Motif)的 NGG 位点,这种特征的序列在每 128bp 的随机 DNA 序列中就重复出现一次。
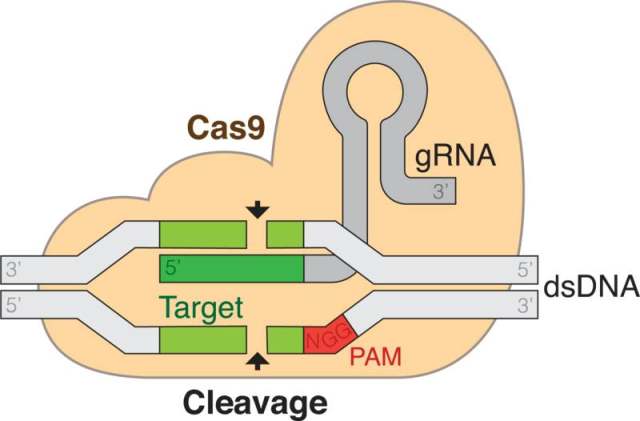
图 4. CRISPR/Cas9 基本结构原理示意图(图片 By Mariuswalter - Own work, CC BY-SA 4.0)
DNA 双链断裂后,在不存在同源模板的情况下发生非同源性末端接合(Non-homologous end joining,NHEJ)修复断裂 DNA。通常在 Cas9 剪切位点附近造成小片段碱基的插入或缺失。如果随机修复发生在基因的编码外显子中,则往往会导致读码框发生移码突变,最终使靶基因无法正常转录翻译。当 DNA 断裂后,细胞核内同时存在与损伤 DNA 同源的 DNA 片段,那么则可通过同源介导的双链 DNA 修复(Homology directed repair ,HDR)在目的位点引入外源 DNA 片段,从而达到片段敲入或编辑的效果。
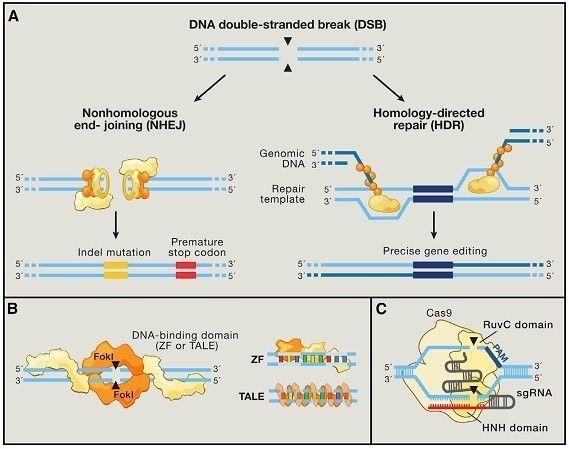
图 5. 利用 DNA 双链断裂修复实现基因定点编辑原理示意图(图片来自 Cell. 2014 Jun 5;157(6):1262-78.)
利用 CRISPR/Cas9 系统的这些特性,CRISPR/Cas9 途径获得基因修饰小鼠模型的主要技术路线:
(1)我们可以针对基因组特定序列设计向导 RNA(gRNA)
(2)体外转录 gRNA 以及编码 Cas9 蛋白的 mRNA
(3)将 gRNA、Cas9 mRNA 注射到小鼠受精卵中
(4)注射后的受精卵移植到假孕母鼠输卵管中,受精卵发育成 F0 代小鼠。
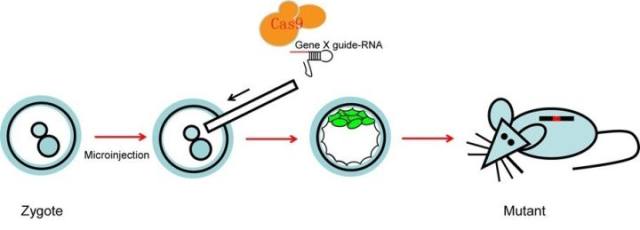
图 6. CRISPR/Cas9 途径获得基因修饰小鼠模型的技术路线(图片来自内部资料)
了解了两大基因定点编辑利器的工作原理,爱思考的你一定会问:如果我要做一种基因修饰小鼠,那么到底应该选择哪种技术呢?
且听我们下回分解!
扩展阅读
正负双向选择系统 (positive-negative-selection, PNS)
由于高等真核细胞内外源 DNA 与靶细胞 DNA 序列自然发生同源重组的机率非常低,约为百万分之一,要把基因敲除成功的细胞筛选出来是一件非常困难的工作。因此,需要借助一些筛选标记来解决这一关键问题。
「+」 正筛选标记:通常是药物抗性基因,最常用的就是 Neo(新霉素抗性基因)。通过构建打靶载体,将带有目的片段的外源 DNA 序列连同正筛选基因 neo 通过 DNA 序列间的同源重组替代基因组中需要敲除或修饰的片段,达到敲除或敲入特定基因的目的。正筛选基因 neo 的表达赋予重组 ES 细胞具有抵抗细胞毒性药物 G418 的特性,使细胞在药物筛选下存活并形成细胞克隆。
「-」 负筛选标记:为减少因随机插入产生的药物抗性克隆对筛选的干扰,可以在打靶载体同源重组区域的外侧加上负筛选基因,通常是细胞毒性相关基因。例如来自疱疹病毒的胸腺嘧啶激酶 (TK) 基因,该基因可以将对细胞无毒的核苷类似物 Ganc 进行磷酸化,从而产生对细胞有毒的核苷酸类似物。 当打靶载体在细胞内进行同源重组时,TK 基因由于在同源重组区域的外侧,因此不会整合到细胞染色体上,随着细胞的生长和分裂 TK 基因发生自然降解和稀释,从细胞中消失。因此这类细胞不会因为 Ganc 的存在而死。但如果发生打靶载体随机插入整合到 ES 细胞染色体上的情况,那么 TK 基因很可能也会同时整合上去,结果导致这类非正确同源重组的 ES 细胞在 Ganc 的存在下生成有毒的核苷酸类似物而致死。
文章来源南模生物,更多技术资料详见:http://c.biomart.cn/modelorg/animal