胃肠间质瘤(GIST)是消化道最常见的间叶源性肿瘤,其发病机制与 KIT 基因和 PDGFRA 基因功能获得性突变相关。KIT 基因突变可引起组织酪氨酸激酶受体通路的激活。PDGFRA 基因是一种酪氨酸激酶 III 型受体,与 KIT 相似,激活突变导致下游多细胞信号转导通路激活,控制重要的细胞功能。
晚期 GIST 患者耐药突变现状
2001 年,芬兰 Joensuu 教授在《新英格兰医学杂志》上报道了 1 例晚期 GIST 病人接受甲磺酸伊马替尼(IM)治疗并取得成功的案例。酪氨酸激酶抑制剂(TKI)伊马替尼成为了治疗晚期不可切除 GIST 的里程碑式药物。然而,随着 IM 在临床上的广泛应用,IM 治疗后的继发性耐药成为临床攻克 GIST 的重大挑战。
研究发现(见图 1),GIST 的原发性突变最常发生于 KIT Exon11, 而继发性突变最可能发生的部位是编码激酶的催化结构域,即编码开关口袋的 KIT Exon13/14、PDGFRA Exon14/15,或是编码激酶活化环结构的 KIT Exon17/18、PDGFRA Exon18。相对于较为单一的原发性突变,继发性突变具有多克隆及多样性的特点。这也为临床治疗晚期 GIST 带来了极大的困难。
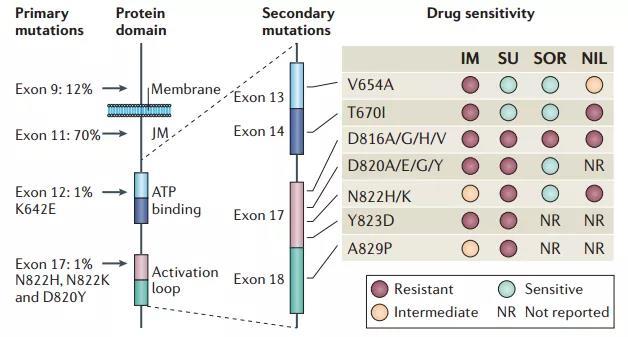
图 1:源于 CorlessC L et al. Nature Reviews Cancer, 2011.
目前,FDA 批准了伊马替尼、舒尼替尼和瑞戈非尼分别作为 GIST 的一线、二线和三线标准疗法。然而,伊马替尼对于 GIST 继发性耐药突变没有任何作用,舒尼替尼仅对 Exon13/14 位点突变有一定效果,瑞戈非尼可显著改善伊马替尼和舒尼替尼治疗后疾病进展的转移性或不可切除 GIST 患者无进展生存期(PFS),为这一难治性患者群带来获益。
然而,随着治疗的进一步深入,患者体内富集的耐药性突变类型更多。
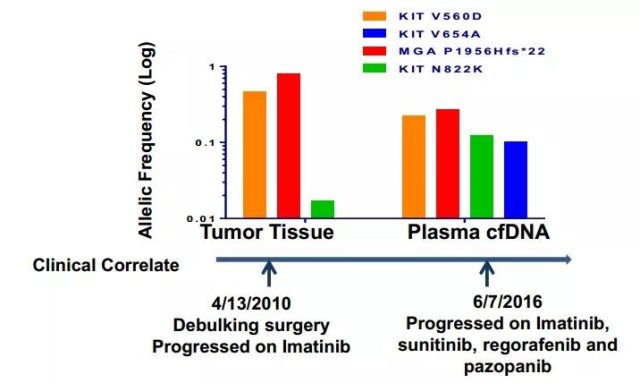
图 2:源于 Kelly/Chi & Reichel/Berger Innovation Lab.
如图 2 中的患者,2010 年其使用伊马替尼治疗后,肿瘤组织中检测出三种耐药性突变。在此后的 6 年间,患者因耐药问题使用了伊马替尼、舒尼替尼、瑞戈非尼、帕唑帕尼多种 TKI 药物,此时患者血浆游离 DNA 不仅可以检出之前已经存在的耐药性突变,同时也出现了新的耐药性突变类型。这类患者的肿瘤治疗过程就如同在玩「打地鼠」游戏,不同类型的耐药性突变如同从不同的洞口探出头的「老鼠」,传统 TKI 药物顾此失彼、束手无策。新型、针对多位点的 TKI 药物才能给 GIST 患者带来新的希望。
瑞派替尼广泛抑制多种耐药突变
瑞派替尼是一种 KIT/PDGFRA 激酶开关调控抑制剂。传统 TKI 药物竞争性结合酪氨酸激酶的 ATP 结合位点,从而抑制酪氨酸激酶活性。瑞派替尼则与受体型酪氨酸激酶的开关口袋结合,从而抑制开关口袋及活化环,将激酶稳定在失活状态,且这种抑制作用不受环境中 ATP 浓度的影响(见图 3)。
图 3:源于 NemunaitisJ et al. Future Oncology, 2020, 16(1): 4251-4264.
在体外激酶实验中,瑞派替尼不仅对野生型 KIT 及 KIT V654A 突变体具有抑制作用,而且对伊马替尼、舒尼替尼、瑞戈非尼耐药的 KIT D816 H 和 D816V 突变体也具有明显的抑制作用。此外,瑞派替尼对野生型 PDGFRα 和 D842V 突变体也具有一定的抑制作用(见图 4)。
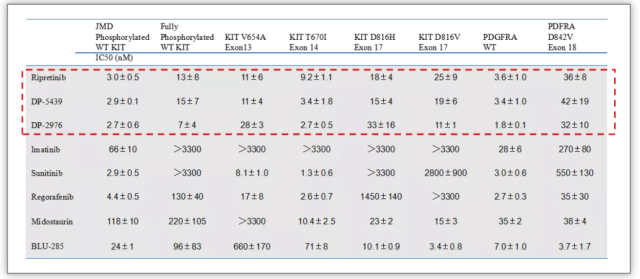
图 4:源于 SmithBD et al., Cancer Cell, 2019.
在 CHO 或 Ba/F3 细胞中转染临床确定的原发性以及药物耐受性 KIT 或 PDGFRA 突变来检测不同种 TKI 药物对不同类型的原发性突变合并耐药性突变的抑制作用。研究结果显示瑞派替尼能够广泛抑制原发 KITExon9/11 突变合并的多种耐药性突变。
图 5 显示的原发 KITExon9 突变合并多种耐药性突变,瑞派替尼对几乎所有类型的继发性突变具有显著的抑制作用,而传统药物中表现最好的瑞戈非尼也仅能对部分继发性突变有抑制作用。
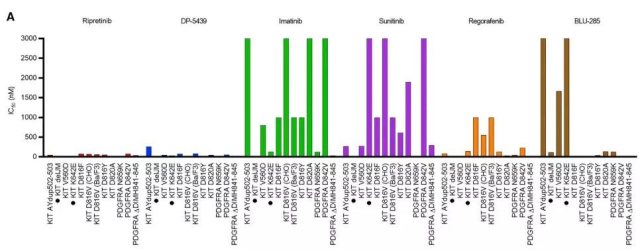
图 5:源于 SmithBD et al., Cancer Cell, 2019.
图 6 显示的是瑞派替尼及其他 TKI 对原发 KITExon11 突变合并多种耐药性突变的抑制效果,瑞派替尼同样对原发 KITExon11 突变合并多种耐药性突变具有广谱的抑制作用。
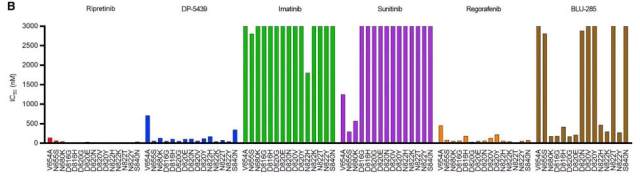
图 6:源于 SmithBD et al., Cancer Cell, 2019.
瑞派替尼临床获益显著
2020 年,LancetOncol 发表了临床试验 INVICTUS 的研究数据(见图 7)。INVICTUS 研究是一项双盲、随机、安慰剂对照Ⅲ期临床研究。研究双盲阶段,既往至少接受过伊马替尼、舒尼替尼和瑞戈非尼治疗的晚期 GIST 患者以 2:1 随机接受瑞派替尼 150 mg 每日 1 次或安慰剂治疗。经盲法独立审查中心确定患者疾病进展后,进入开放研究阶段,安慰剂组患者在疾病进展后可以交叉至瑞派替尼 150 mg 每日 1 次组进行治疗。研究的主要终点为根据 MRECIST1.1 标准评估的 PFS,次要终点包括总生存期(OS)、研究者评估的 PFS、生活质量(QOL)和安全性等。
INVICTUS 结果显示,瑞派替尼中位 PFS 为 6.3 个月,而安慰剂组中位 PFS 是 1.0 个月。进一步分析安慰剂组中交叉接受瑞派替尼治疗和未接受瑞派替尼治疗的患者,交叉治疗可以带来显著的 OS 获益,两组中的 OS 分别为 11.6 个月和 1.8 个月。
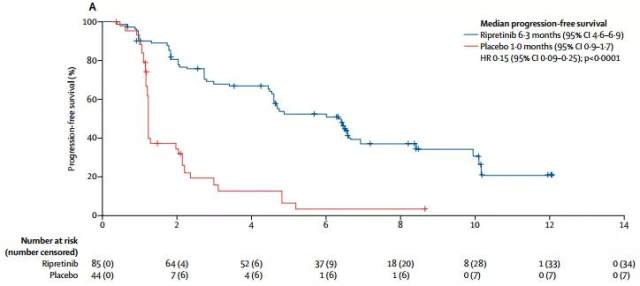
图 7:源于 BlayJB, et al. Lancet Oncol, 2020.
治疗组较安慰剂组显著改善 OS,中位 OS 分别为 15.1 个月和 6.6 个月(见图 8)。
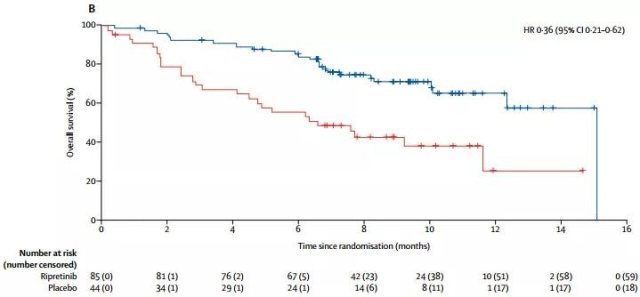
图 8:BlayJB, et al. Lancet Oncol, 2020.
在安全性和耐受性方面瑞派替尼表现同样出色,瑞派替尼组患者多出现的是 1 级和 2 级不良反应事件,例如脱发、肌痛、恶性、疲劳、掌趾红细胞感觉异常综合征、便秘、食欲下降、体重下降、血胆红素升高、关节痛、肌肉痉挛等。与已上市的 TKI 相比,瑞派替尼的副作用风险均较低,很少有患者需要降低药物剂量或中断治疗,耐受性良好。
瑞派替尼组患者在治疗期间的生活质量和身心健康得到明显改善(见图 9),其 EQ-5D-5L 视觉模拟评分表现为增加,而安慰剂组表现为下降(P = 0.004)。EORTCQLQC30 评分瑞派替尼组表现为躯体功能和角色功能的改善,而安慰剂组表现为恶化(P = 0.004;P = 0.001)。患者接受瑞派替尼治疗对比安慰剂治疗,表现为总体健康状况和总体生活质量的改善,差异具有临床意义,也有显著统计学意义(P = 0.001;P = 0.001)。
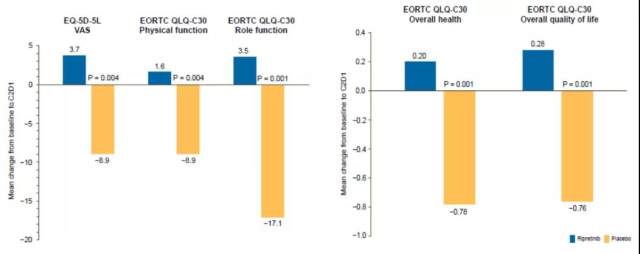
图 9:源于 HeinrichMC, et al. ASCO2020, Abstract No.11535.
综上,瑞派替尼能够为晚期 GIST 患者带来显著的临床获益,且安全性和耐受性良好。瑞派替尼已获 FDA 批准用于晚期 GIST 的四线治疗。最新的 2020 版 NCCN 指南与 2020 版 CSCOGIST 指南也将瑞派替尼推荐作为四线的标准治疗。瑞派替尼未来临床应用前景值得期待!
参考文献:
1.Nemunaitis J, Bauer S, Blay J, et al. Intrigue: Phases Ⅲ study ofripretinib versus sunitinib in advanced gastrointestinal stromaltumor after imatinib[J]. Future Oncology, 2020, 16(1): 4251-4264.
2.Corless C L, Barnett C M, Heinrich M, et al. Gastrointestinal stromaltumours: origin and molecular oncology[J]. Nature Reviews Cancer,2011, 11(12): 865-878.
3.Blay J Y, Serrano C, Heinrich M C, et al. Ripretinib in patients withadvanced gastrointestinal stromal tumours (INVICTUS): a double-blind,randomised, placebo-controlled, phase 3 trial[J]. The LancetOncology, 2020.
内容审核:赵夕玥
题图来源:站酷海洛