小测试:
如果有两组数据摆在你的面前,针对同一类患者(基线特征相似,但不完全一致),究竟是 A 方案更好,还是 B 方案更好呢?
A 方案:PD-1 抑制剂 1
mPFS: 9.0 vs 4.9
HR:0.48
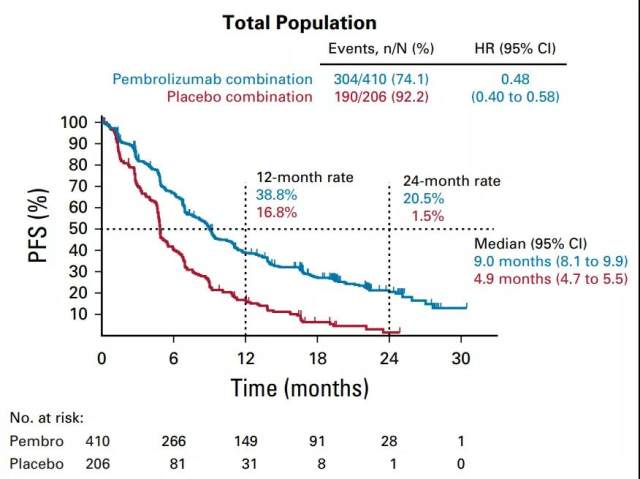
B 方案:PD-1 抑制剂 2
mPFS: 11.3 vs 8.3
HR:0.60
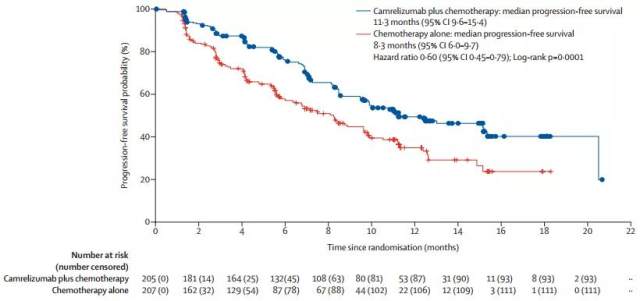
临床研究中的两个关键疗效指标,到底应该看中位值(PFS/OS)大小,还是看 HR 值(风险比)大小?
肿瘤免疫治疗研究火热,进展层出不穷,由于缺乏头对头对比,我们往往通过间接比较设计相近的研究来「大概判断」不同治疗方案的优劣。而经常被我们「直接」拿来比较的就是中位值,最常见的就是总生存期(OS)和无进展生存期(PFS)。
中位值的优势和劣势 [1]
中位值就是将一组数据按大小顺序排列,处在最中间位置的那个数。其最大的有点就是简单直观,但也会受到诸多因素的影响。
1. 受数据结构的影响:
如果数据是偏态分布,则中位值就不能很好的代表患者的总体生存获益;通常临床试验的研究数据来自纵向观察或随访,而这类数据基线状态差异较大,不服从正态分布,且不可避免存在着数据的删失 [1]。这也会导致通过中位生存时间来比较两组患者的生存情况不够准确。
2. 受数据成熟度的影响:
如果数据没有成熟,也就是说数据的成熟度不到 50%,那就无法计算出中位值,于是中位值就会「开天窗」,最终的结果就是 NR(not reach),即未达到。
3. 肿瘤免疫治疗的特点:
以肿瘤免疫治疗为代表的新型治疗策略,旨在激活机体自身的免疫功能,这是一个缓慢起效的过程,因此免疫治疗存在「长拖尾效应」,只有当患者接受一段时间的治疗后,才能持续、稳定地从免疫治疗中获益,这就导致了数据分布更加偏态。如果仅仅关注中位值来进行终点治疗的比较,在当下的肿瘤免疫治疗时代中,显然具有较大的局限性。
简言之,有代表性的中位值对数据要求较高,且对于肿瘤免疫治疗来说具有一定的局限性。因此,如果你还是只关注生存曲线上的一个点,而不关注生存曲线上的其他点,显然会对临床研究的数据照成极大的浪费,既不全面也不科学。
HR 的优势和劣势 [1]
HR(Hazard Ratio,风险比)是通过 COX 比例风险回归模型计算得出的一个相对指标,用以量化两条生存曲线之间的整体差异。举个例子,想要比较新治疗方案 A 和标准治疗方案 B 对于晚期肿瘤患者的治疗效果,可能会有以下几种结果:
① 新治疗方案 A 对比标准治疗方案 B,HR < 1(例如 HR = 0.60),且 P 值有显著的统计学意义(如 P < 0.05),可以解释为:相比标准治疗方案 B,新治疗方案 A 的疗效更好,可显著降低 40% 的疾病进展或死亡风险。
② 新治疗方案 A 对比标准治疗方案 B,HR = 1,可以解释为:新治疗方案 A 的疗效和标准治疗方案 B 的疗效没有显著的差异
③ 新治疗方案 A 对比标准治疗方案 B,HR > 1(例如 HR = 1.20),且 P 值有显著的统计学意义(如 P < 0.05),可以解释为:相比标准治疗方案 B,新治疗方案 A 的疗效更差,会增加 20% 的疾病进展或死亡风险 [2]。
看起来比较复杂,那 HR 值的优势在哪里呢?
1. 受数据结构和数据成熟度的影响较小:
HR 对于研究数据的要求较低,即使是偏态分布或删失较多的数据,都可以进行计算,且 HR 的结果受到个别患者状态的影响较小 [3];
2. 结果更全面更稳定:
HR 会使用截止到数据分析时已经产生的所有数据,分析更加全面和稳定;而中位值只能反应某个点的数据 [2],不但浪费了大量临床研究的数据,而且往往会夸大或者低估获益,尤其在免疫肿瘤时代,由于存在明显的拖尾效应,使用中位值会严重低估免疫治疗的获益。
3. 适合不同研究之间的间接对比:
HR 可通过多变量 COX 比例风险回归模型调整去除混杂因素的影响 [2],更适合不同研究之间的间接对比。
当然,HR 值作为一个相对值,它受分母影响较大。有很多研究,HR 值看起来差异很大,但主要是对照组表现不佳,实际上试验组也没有很好。
小 tips:文章开头两个临床研究中的 P 值,反映的是 HR 值的 95% 置信区间上限「有统计学意义的」< 1,但我们不能说这两个中位 PFS 有显著的统计学差异,这是一个我们经常会犯的错误。
目前已经上市的 PD-1/L1 抑制剂,HR 值比比看?
目前大部分临床研究都会同时给出中位生存期和 HR 值。中位值虽然更加直观,但在使用时的局限性较多,而 HR 值能很好的避免这些局限性,所以在解读这些数据的时候,我们应该把中位值和 HR 值综合起来一起看,才能更好的解读这些终点数据。
仍然以肿瘤免疫治疗为例,目前我国已获批的几种 PD-1/L1 抑制剂一线治疗晚期非鳞状非小细胞肺癌时的疗效数据汇总如下,感兴趣的同学可以再重新审视一下这些临床研究的结果 [4~8]:
在靶向治疗和免疫治疗研究进展层出不穷的今天,由于缺乏头对头的直接对比,直接比较不同研究的中位值显然是不够科学的,我们更应该关注这些研究的 HR 值,可以相对更科学的评估不同研究间不同药物的可能差异,从而为我们制定治疗决策提供相关信息。PP CEJ CHN 10
参考文献
[1]. 王权, 等. 风险比在生存资料 Meta 分析中的应用. 中国循证心血管医学杂志. 2013;5(6):559-560.
[2]. Barraclough H, et al. Biostatistics primer: what a clinician ought to know: hazard ratios. J Thorac Oncol. 2011 Jun;6(6):978-82.
[3]. 安胜利, 姜立. 正确理解临床试验中的风险比. 循证医学. 2010;10(3):186-187.
[4]. Gadgeel S, et al. Updated Analysis From KEYNOTE-189: Pembrolizumab or Placebo Plus Pemetrexed and Platinum for Previously Untreated Metastatic Nonsquamous Non-Small-Cell Lung Cancer. J Clin Oncol. 2020;38(14):1505-1517. doi:10.1200/JCO.19.03136
[5]. Zhou C, et al. Camrelizumab plus carboplatin and pemetrexed versus chemotherapy alone in chemotherapy-naive patients with advanced non-squamous non-small-cell lung cancer (CameL): a randomised, open-label, multicentre, phase 3 trial. Lancet Respir Med. 2021;9(3):305-314. doi:10.1016/S2213-2600(20)30365-9
[6]. Zhang L. ORIENT-11: Sintilimab + Pemetrexed + Platinum as First-Line Therapy for Locally Advanced or Metastatic Non-Squamous NSCLC. Presented at WCLC 2020 - Virtual Presidential Symposium.
[7]. Lu S, et al. Tislelizumab Plus Chemotherapy as First-Line Treatment for Locally Advanced or Metastatic Nonsquamous NSCLC (RATIONALE 304): A Randomized Phase 3 Trial [published online ahead of print, 2021 May 23]. J Thorac Oncol. 2021;S1556-0864(21)02176-6. doi:10.1016/j.jtho.2021.05.005
[8]. Socinski MA, et al. IMpower150 Final Overall Survival Analyses for Atezolizumab Plus Bevacizumab and Chemotherapy in First-Line Metastatic Nonsquamous NSCLC. J Thorac Oncol. 2021 Jul 24:S1556-0864(21)02322-4.