T 细胞大颗粒淋巴细胞白血病(T-cell Large Granular Lymphocyte Leukemia,T-LGLL)是一种较为罕见的 T 淋巴细胞克隆性疾病,主要由细胞毒性 T 淋巴细胞克隆性增殖引起,诊断主要依靠临床病史、细胞形态学、流式免疫分型、TCR 基因重排[1]。流式细胞术在诊断 T-LGLL 中可以明确是否存在表型异常大颗粒淋巴细胞,并对其克隆性进行判断[2]。典型 T-LGLL 的免疫表型为 CD3+CD8+CD57+CD56-TCRαβ+ 同时伴有 T 系抗原 CD2、CD5、CD7 的表达减弱或者缺失[2,3],少见表型有 CD3+CD4+CD8-CD57+CD56-TCRαβ+,CD3+CD4-CD8-CD57-CD56-TCRγδ+[3]。少数病例可有 CD56 的表达,CD56 的表达被报道与疾病的侵袭性表现相关[2,4,5]。
临床资料
1.1 病史及体格检查
患者男性,66 岁,主诉「摔伤后咳嗽咳痰 6 天,发现淋巴细胞升高 4 天」入院。入院六天前不慎摔伤头部、胸部等处收治入外科,入院后出现咳嗽、咳痰症状,血常规检查发现淋巴细胞升高,后进一步转入血液科治疗。入院查体:体温 37.1 ℃,脉搏 87 次/min,呼吸 20 次/min,血压 168/76 mm Hg(1 mm Hg = 0.133 Kpa)。患者神志清楚,头部擦伤,浅表淋巴结未及肿大。右胸部压痛,胸廓挤压征(+),双肺呼吸音清,未闻及干湿啰音,腹平软,无压痛反跳痛,未触及包块,肝脾肋下未及,双肾区无叩痛,移动性浊音阴性,肠鸣音 4 次/分。右肩压痛抬举稍受限,余肢活动可。
1.2 实验室及辅助检查
1.2.1 血常规及血生化检查
血常规示白细胞计数(WBC)14.11×109/L,中性粒细胞计数 8.63×109/L,淋巴细胞计数 4.88×109/L,中性粒细胞百分比 61.2%,淋巴细胞百分比 34.6%,红细胞计数(RBC)4.03×109/L,血红蛋白(Hb)132 g/L,平均红细胞体积(MCV)95 fl,血小板计数(PLT)PLT 194×109/L。球蛋白 25.4 g/L,乳酸脱氢酶(LDH)141 U/L。HBV(-) ,HCV(-),EBV-DNA(-),CMV-DNA(-),ANA(-),RF(-)。
1.2.2 骨髓相关检查
外周血涂片(如图 1)可见颗粒淋巴细胞,胞浆较丰富,嗜碱性,部分可有伪足状突起,可见大小不等的嗜天青颗粒。骨髓涂片(如图 2):涂片增生尚活跃,粒系相对增生,红、巨二系增生减低。淋巴细胞比例偏高,细胞形态与外周血一致。
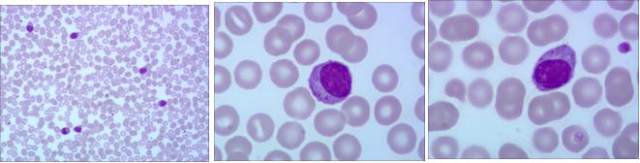
图 1 外周血涂片(瑞氏染色,×1000)
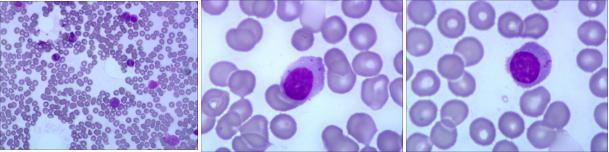
图 2 骨髓涂片(瑞氏染色,×1000)
1.2.3 骨髓流式免疫分型
采用 Beckman Coulter FC500 流式细胞仪进行免疫分型。应用 FCS 软件进行分析。淋巴细胞约占 44.6%,可见约 40.4% CD3+CD5-CD7- T 细胞,免疫表型为 CD3+,CD4-,CD8+,CD56 部分+,CD2+,CD5-,CD7-,CD57-,CD16-,TCRαβ+,TCRγδ-。免疫分型图如图 3 所示。
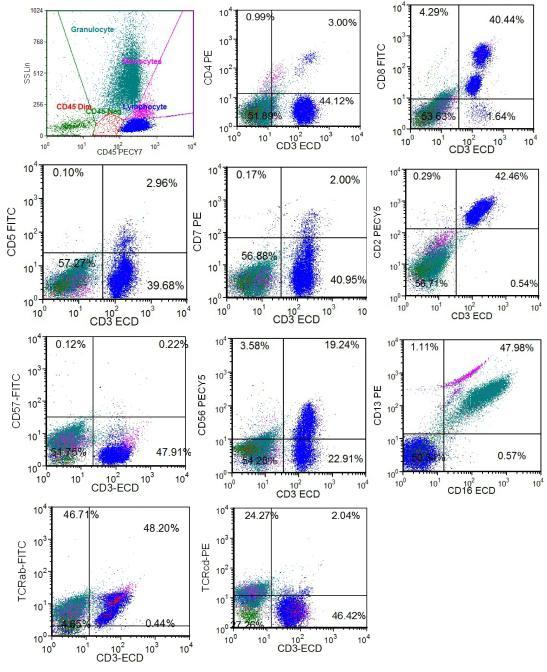
图 3 患者骨髓流式免疫表型
1.2.4 T 细胞受体 β 链受体库(TCR-Vβ)检查及 TCR 基因重排
采用 Beckman Coulter 的 TCR-Vβ 库试剂盒以及 FC500 流式细胞仪进行 TCR-Vβ 检测。送检标本中可见成熟 T 细胞约占有核细胞总数约为 32.8%,可见 Vβ8 片段的限制性扩增,约占 CD3+ T 细胞的 87.26%,提示存在单克隆 T 细胞(图 4)。TCR 基因重排检测不成功。
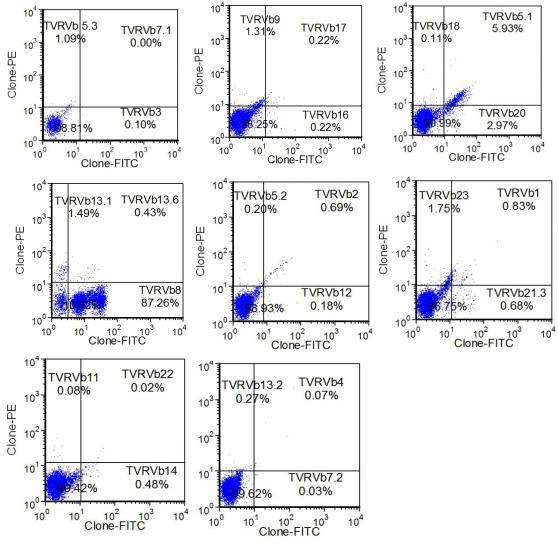
图 4 患者骨髓 T 细胞受体 β 链受体库(TCR-Vβ)检查
1.2.5 淋巴结 B 超
双侧腹股沟见数个椭圆型低回声光团,边缘光整,内部回声欠均匀,可见血流信号,左侧较大 12×4 mm,右侧较大 12×5 mm。
2 讨论
2.1 T-LGLL 的诊断
诊断要求:
1、持续存在 T-LGL 细胞。2016 年 WHO 造血与淋巴组织肿瘤分类及诊断标准中,T-LGL 细胞持续存在时间超过 6 个月,绝对数在 2~20×109/L[6]。但文献报道,克隆性 T-LGL 绝对数 <2×109/L 的病人临床表现与 >2×109/L 的病人类似[7,8]。有报道认为,只要病人表现出血细胞减少(例如粒缺或者贫血),并且存在克隆性扩增的 T 淋巴细胞,绝对数在 0.4~2×109/L,仍然可以考虑 T-LGLL 的诊断[9,10]。
2、特征性的免疫表型[7]。典型的免疫表型为 CD3+CD8+CD57+CD56-TCRαβ+ 同时伴有 T 系抗原 CD2、CD5、CD7 的表达减弱或者缺失。少见表型如 CD3+CD4+CD57+CD8-/dim+ 可以出现在 10%~15% 的病例中[9],此外还可表现为 CD3+CD4-CD8-CD57-CD56-TCRγδ+[3,10]。CD56+ 的 T-LGLL 比较少见,临床经常呈现侵袭性表现[4,5]。此类病人临床进展快,发病初期伴有 B 症状(发热、盗汗、体重减低)、肝脾肿大和血细胞减少,实验室检查中 LGL 数目偏高大于 0.5×109/L,经常大于 10×109/L,对传统治疗反应不敏感,类似急性淋巴细胞白血病的诱导化疗方案,预防性鞘注,以及大剂量巩固化疗和造血干细胞移植可能可以改善预后[5]。但仍需注意的是,CD56 阳性并不代表患者临床表现一定为侵袭性,部分惰性 T-LGLL 病例中也可以伴随 CD56 的表达,同时也有临床表现呈侵袭性的患者 CD56 阴性[10]。
3、T 细胞克隆性[7]。由于病毒感染或其它因素也可导致 LGL 细胞的扩增,在诊断 T-LGLL 时必须明确扩增的 LGL 是否为克隆性。可以根据流式 TCR Vb 检测或者 TCR 基因重排来进行 T 细胞克隆性的判断[7,9]。
4、典型的临床表现。T-LGLL 发病中位年龄在 60 岁左右,男女发病率相当[7,9]。有 1/3 的人无明显临床表现,在体检进行血细胞计数时被偶然发现[9]。主要的临床表现有:贫血,细菌感染和疲劳,脾大导致的腹部不适。很多病人伴随自身免疫性相关疾病,17%~37% 的病人有类风湿性关节炎的病史,41%~57% 的病人类风湿因子阳性[9]。除了最常见的类风湿关节炎以外,其它自身免疫性疾病,例如系统性红斑狼疮、干燥综合征、多发性肌炎、乔本氏甲状腺炎和自身免疫性溶血性贫血均有报导,部分病人可以出现纯红再障表现(pure red cell aplasia,PRCA)[8,9]。国内国外患者临床表现有差异,有研究发现,国内患者贫血相关症状表现突出,27 例 T-LGLL 中有 77.8% 出现贫血(66.7% PRCA),无一例合并类风湿关节炎或干燥综合征;而国外研究中该发生 PRCA 的比例在 7%~9%[8]。大约 2/3 的病人在病程中会出现白细胞减少、反复细菌感染、自身免疫紊乱和脾大[7,9,10];20%~40% 的病人会因白细胞减少,出现反复的感染;20%~40% 的病人会出现 B 症状(发热、盗汗、体重减轻);20%~50% 的病人会出现中重度脾肿大;10%~20% 的病人会出现肝肿大;病人不大会出现淋巴结肿大[7]。根据临床病程,可分为惰性或者侵袭性,侵袭性 T-LGLL 的表现与侵袭性 NK-LGLL 表现类似[7]。
2.2 T-LGLL 发生的分子机制
大颗粒淋巴细胞(Large Granular Lymphocyte,LGL)是指细胞形态上描述的胞浆中有嗜天青颗粒的大淋巴细胞。正常人中,大颗粒淋巴细胞约占外周血单个核细胞的 10%~15% 左右[7,10]。根据免疫表型的不同,分为自然杀伤细胞(Natural Killer cells,NK)和 T 细胞。NK 细胞 CD3 为阴性,约占大颗粒淋巴细胞的 85%;T 淋巴细胞约占 15%,主要是经过抗原刺激过的 CD3+CD8+ 细胞毒 T 淋巴细胞(Cytotoxic lymphocyte,CTL)[7]。LGL 可以在多种情况下出现扩增,呈反应性或者克隆性表现。病毒感染后,例如巨细胞病毒(Cytomegalovirus,CMV)及成人 T 淋巴细胞白血病病毒(Human T-lymphotropic Virus 1,HTLV-1)感染;在自体或异基因造血干细胞移植以后、使用酪氨酸激酶抑制剂(Tyrosine Kinase Inbibitor,TKI)之后,也可以出现单克隆或者多克隆 LGL,但是这种情况下出现的颗粒淋巴细胞的扩增与细胞减少无关,所以不需要治疗[10]。克隆性 LGL 扩增原因目前未知,有文献称,反复受 MHC I 类分子的刺激,会导致 CTL 细胞的克隆性扩增[10]。大颗粒淋巴细胞白血病(Large Granular Lymphocyte Leukemia,LGLL),就是 LGL 克隆性增殖的疾病,约占 T/NK 肿瘤的 2%~5%[7] 左右。根据细胞来源的不同,分为两个疾病实体,NK-LGLL 和 T-LGLL[7,9],目前 NK-LGLL 在 2008 和 2016 WHO 造血与淋巴组织肿瘤分类及诊断标准中命名为慢性 NK 细胞增殖症[9]。T-LGLL 是最常见的 LGL 慢性增殖性疾病,在西方国家诊断病例中,约占 LGLL 的 85%~90%[7]。虽然 T-LGLL 发病的具体分子机制未知,但是促凋亡通路如鞘磷脂和 Fas/FasL 的抑制,和存活通路如 MAPK-ERK-ras,NF-κB 及 PI3K/Akt 的活化被报道与其相关[8,9]。近年来,有研究发现,在 11%~73% 的病人中,可见 JAK-STAT 信号通路下游的活化信号传导与转录激活因子3(Activated signal transducer and activator of transcription 3,STAT3)突变,导致 STAT3 的持续活化和下游基因的激活[9]。与无突变病人相比,有 STAT3 基因突变的病人更容易出现白细胞减少和风湿性关节炎的表现[10]。此外,STAT5b SH2 结构域的突变也在 <5% 的 LGLL 病人中被发现[9,10],有文献报道称具有 STAT5b 突变的患者在临床表现上更具侵袭性[9]。自体的或者外源性的抗原刺激是 LGL 克隆性扩增的始发因素,LGL 细胞受抗原刺激后大量扩增,某些凋亡通路的抑制及活化通路的持续活化,导致细胞不能及时凋亡,最后演变为克隆性的扩增。
2.3 T-LGLL 的治疗
T-LGLL 的治疗主要基于病例报道和回顾性队列分析研究[7]。大多数 T-LGLL 是慢性和惰性的病程,预后较好,中位生存期可以达到 10 年以上。尽管有 60% 的病人在疾病发展过程中需要治疗,仍有约 30% 的病人在疾病初期不需要治疗,每 3 到 6 个月监测随访一次即可[7,9]。开始治疗的指征包括:威胁生命的感染、严重的粒细胞缺乏、输血依赖性贫血、血小板减少、严重的 B 症状、迅速增加的循环淋巴细胞[7,9]。由于缺乏大的前瞻性队列研究,目前暂无 T-LGLL 一线治疗的指南,大多数病人起始治疗都是使用免疫抑制剂,例如甲氨蝶呤、环磷酰胺和环孢霉素[7,9,10]。甲氨蝶呤(10 mg/m2/周),客观缓解率(Objective Response Rate,ORR)在 56%,起效时间各有不同,一般认为使用 4 个月后需要再次评估治疗反应[9]。环磷酰胺(50~100 mg/天,口服),口服环磷酰胺首先发现在少数伴随纯红再障的 T-LGLL 病人中有效[9],ORR 约为 71%,反应中位时间约为 4 个月;由于长期服用存在潜在发展为 MDS 或者急性白血病的风险,一般建议使用时间不超过 12 个月[9]。环孢霉素 A(5~10 mg/kg/天,口服),剂量可以根据患者肾功能情况及血液学反应进行调整,ORR 为 56% 左右[9]。靶向治疗主要针对活化信号通路上的相关分子,例如 Tipifarnib,Tofacitinib,Bortezomib,PI3K 抑制剂等[9]。对于少数侵袭性 T-LGLL 的病人,由于预后不佳,进展较快,治疗反应差,文献建议使用类似急性淋巴细胞白血病诱导方案,后续大剂量化疗及造血干细胞移植进行巩固治疗[5]。
总之,T-LGLL 是一类比较少见的 T 细胞克隆性增殖性疾病,临床表现有一定差异,需完善实验室检查及基因突变检查,进行个体化的预后分层及个体化的治疗。
参考文献
[1]National Comprehensive Cancer Network. NCCN[Z], 2014.
[2] Jevremovic D, Olteanu H. Flow Cytometry Application in the Diagnosis of T/NK-cell Lymphoproliferative Disorders[J]. Cytometry Part B 2019,9999(B):1-17.
[3] 林果为等.现代临床血液病学 [M].上海:复旦大学出版社,2013.
[4]Gentile TC, Uner AH, Hutchison RE, et al. CD3+,CD56+ aggressive variant of large granular lymphocyte leukemia[J]. Blood, 1994, 84(7): 2315-2321.
[5]Alekshun TJ, Tao J, Sokol L. Aggressive T-cell large granular lymphocyte leukemia:a case report and review of the literature[J]. Am J Hematol, 2007, 82(6): 481-485.
[6]H SH, Campo E, Harris NL, et al. WHO classification of tumours of haematopoietic and lymphoid tissues(revised 4th edition).IARC:Lyon[Z], 2017.
[7]Sokol L, Loughran TP, Jr. Large granular lymphocyte leukemia[J]. Curr Hematol Malig Rep, 2007, 2(4): 278-282.
[8] 王文生.纯红细胞再生障碍性贫血与 T 细胞大颗粒淋巴细胞白血病 [J].中华临床医师杂志: 电子版,2014(22):4086-4091.
[9]Matutes E. Large granular lymphocytic leukemia. Current diagnostic and therapeutic approaches and novel treatment options[J]. Expert Rev Hematol, 2017, 10(3): 251-258.
[10] Oshimi K. Clinical features, Pathogenesis And treatment of large granular lymphocyte leukemias[J]. Intern Med, 2017, 56(14): 1759-1769.