一、主诉
男性,31 岁,发现表面抗原阳性 20 余年,肝功异常 10.5 年。
二、治疗过程及疗程
10.5 年前(2009-10-14)开始出现肝功异常,ALT 75 U/L,HBV DNA 2.3×10^8 IU/ml(国产,检测下限 <100IU/ml),给予短效干扰素 600 万 U 隔日一次联合拉米夫定 100 mg qd 抗病毒治疗,治疗 3 个月复查,ALT 33 U/L,HBV DNA 1.96×10^4 IU/ml,治疗 10 个月时 HBV DNA 上升至 7.57×10^5 IU/ml,治疗 13 个月(2010-11)时 HBV DNA 1.09×10^4 IU/ml , 仍为 E 抗原阳性,停用干扰素,继续单用拉米夫定,2011 年 9 月自行停药。2015-1 曾复查 ALT 50 U/L,未进一步检查。
2017 年 6 月复查,ALT 69 U/L,HBV DNA 8.3×10^7 IU/ml,当时未治疗,2017-9 复查,ALT 152 U/L,HBV DNA >3×10^8 IU/ml,开始再次启动抗病毒治疗,选择替诺福韦 TDF 300 mg qd,治疗 3 个月(2017-12-5)时复查,ALT 72 U/L,HBV DNA 8.39×10^5 IU/ml,治疗 8 个月(2018-4-29)时复查,ALT 119 U/L,HBV DNA 1.42×10^6 IU/ml,考虑疗效不佳,抗病毒方案更改为替诺福韦联合恩替卡韦 ETV 0.5 mg qd,联合治疗 1 个月时 HBV DNA 降至 1.25×10^4 IU/ml,联合治疗 4 个月(2018-8-28)复查,ALT 上升至 215 U/L,HBV DNA 上升至 8.39×10^5 IU/ml,抗病毒治疗方案调整为停用 TDF,单用 ETV,期间(2018-8-28 至 2019-6-23)ALT 波动于 174~258 U/L,HBV DNA 波动于 1.67~7.88 ×104IU/mL,HBsAg 定量 26039~20502 IU/ml,2019 年 6 月加用丙酚替诺福韦 TAF 丙酚替诺福韦 25 mg qd,联用 1 个月(2019-7-20)复查,ALT 167 U/L,HBV DNA 4.02×10^2 IU/ml,联用 6 个月(2020-1-7)复查,ALT 100 U/L,HBV DNA 1.6×10^2 IU/ml,HBsAg 定量下降至 12483 IU/ml。
抗病毒多年,肝弹性检测仍在正常范围,且无进展。
不良反应监测:抗病毒多年,肾功能 Scr 波动在 56~70umol/L, 血磷水平波动在 1.15~1.39 mmol/L,无异常。出现 CK 升高问题:抗病毒之前未查 CK,服 TDF 3 个月后(2017.12)感轻度乏力,查 CK 985 U/L, 停止健身 10 天后复查,CK 反而升高至 2292 U/L,肌红蛋白 325 ng/ml,后 CK 逐渐回落,2018-3 至 2018-8-28 含替诺福韦的治疗方案期间,CK 波动在 690~1046 U/L,单用恩替卡韦期间 CK 波动在 1043~1105 U/L,加用丙酚替诺福韦半年时(2020-1-7)CK 上升至 2208 U/L。此过程中肌肉无力症状轻微,总体感觉肌肉爆发力差,耐力可。神经科查体无异常。
第二次抗病毒期间(2017-9 至今)ALT 和 HBV DNA 的变化如图 1,CK 及 HBsAg 定量的变化如图 2
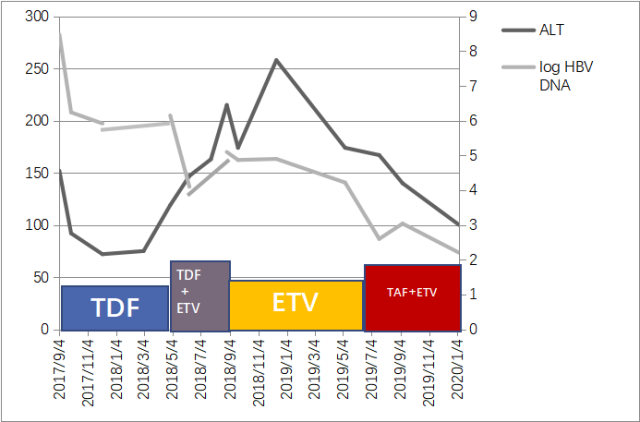
图 1:抗病毒期间(2017-9 至今)的 ALT 和 HBV DNA 变化
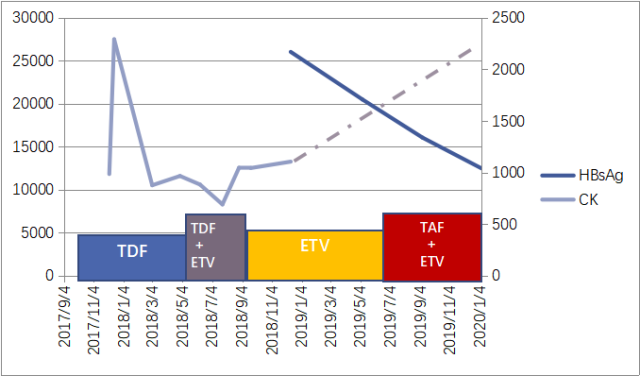
图 2:抗病毒期间(2017 年 9 月至今)的 CK 和 HBsAg 定量的变化
三、个人史
有吸烟史,饮酒史。3 年前戒酒。
四、家庭史
母亲为乙肝病毒感染者,否认肝硬化肝癌家族史。
五、治疗体会
该年轻男性患者,抗病毒治疗过程较复杂,对多种抗病毒药物,如干扰素、TDF、ETV 甚至 TDF 联合 ETV 均疗效不佳,推测可能与其乙肝病毒准种较复杂或者存在某些位点突变有关。遗憾的是,暂未进行这方面的检测。
更改为 TAF 丙酚替诺福韦联合 ETV 的治疗方案后,才出现 HBV DNA 的明显下降,ALT 及 HBsAg 也较前降低,体现出 TAF 丙酚替诺福韦更加强效的抗病毒作用。它的强效作用与药物自身良好的特性有关。TAF 丙酚替诺福韦不在血液中水解,而是在进入肝脏细胞以后才会水解成为替诺福韦,并进一步被双磷酸化后成为双磷酸替诺福韦,发挥抗病毒作用。TAF 丙酚替诺福韦具有一定的靶向性,使得较低剂量的 TAF 丙酚替诺福韦(25 mg)就能代谢为足够浓度的细胞内双磷酸替诺福韦发挥抗病毒效力。也正是因为 TAF 丙酚替诺福韦的靶向性及入胞后才水解的特性,TAF 丙酚替诺福韦在血浆中稳定性高(半衰期为 31 分钟)且浓度低,血液中暴露的 TFV 经由循环进入肾小管的量也因此大幅度降低(相比 TDF 降低 89%),因此提高了 TAF 丙酚替诺福韦的肾脏安全性,也大大降低了基于肾小管损害而发生的骨密度降低的风险。本患者使用过多种抗病毒药物,但年纪较轻,未出现肾脏方面的不良反应。当然,随着治疗时间的延长,也应进一步监测是否出现影响肾脏安全性的问题。
此外,该患者在抗病毒过程中出现 CK 升高的问题,虽然症状较轻,但却贯穿全程,值得引起关注。在最初使用 TDF3 个月时 CK 最高达 13 倍正常值上限,后又逐渐降低,波动在 4 倍至 5.5 倍正常值上限,停用 TDF 单用 ETV 期间 CK 也在 6 倍正常值上限左右,加用 TAF 丙酚替诺福韦后上升至 12.7 倍正常值上限。由此可见,该患者对多种核苷类药物的肌肉损伤比较易感,应继续监测 CK 变化及患者的症状,避免进一步加重。在 TAF 丙酚替诺福韦的Ⅲ期临床试验中 [1,2],TAF 丙酚替诺福韦以及 TDF 在治疗 48 周内 CK 出现 4 级升高(≥ 10ULN)的发生率均为 3%。在另外一项前瞻性的对照研究中 [3],最长治疗至 240 周,替比夫定和恩替卡韦发生 CK 升高的比例分别是 67% 和 12.1%,发生 3/4 级(≥ 7ULN)的 CK 升高的比例分别是 9.3% 和 5.1%。因此,除替比夫定外,其他核苷类抗病毒药物的肌肉损害也值得关注。
参考文献:
1. Chan HL, Fung S, Seto WK, et al. Tenofovir alafenamide versus tenofovir disoproxil fumarate for the treatment of HBeAg-positive chronic hepatitis B virus infection: a randomised, double-blind, phase 3, non-inferiority trial. Lancet Gastroenterol Hepatol. 2016;1(3):185-195.
2. Buti M, Gane E, Seto WK,et al. Tenofovir alafenamide versus tenofovir disoproxil fumarate for the treatment of patients with HBeAg-negative chronic hepatitis B virus infection: a randomised, double-blind, phase 3, non-inferiority trial. Lancet Gastroenterol Hepatol. 2016;1(3):196-206.
3. Zhang Y, Hu P, Qi X, et al. A comparison of telbivudine and entecavir in the treatment of hepatitis B e antigen-positive patients: a prospective cohort study in China. Clin Microbiol Infect. 2016 ;22(3):287.
