近年来,靶向治疗在驱动基因阳性的非鳞非小细胞肺癌(NSCLC)患者中取得了巨大成就,但是对于占全部肺癌 30%~40% 的鳞状 NSCLC(肺鳞癌)[1],由于较少发现可明确做为药物靶点的驱动基因,因此,晚期肺鳞癌的治疗仍以化疗为主 [2]。免疫治疗的出现改变了这一现状,2019 年 11 月,帕博利珠单抗联合含铂化疗一线治疗转移性鳞状 NSCLC 的适应证在国内获批,为晚期肺鳞癌患者带来了全新的治疗策略。
在近期举行的第一届默沙东肿瘤高峰论坛上,华中科技大学同济医学院附属协和医院董晓荣教授和复旦大学附属肿瘤医院放射治疗科主任医师朱正飞教授接受了记者采访,详细讲述了免疫治疗对晚期肺鳞癌治疗格局的影响、国内晚期 NSCLC 免疫治疗现状和免疫治疗药物的选择及疗效判断方法。
免疫联合化疗一线治疗肺鳞癌有望成为临床实践新标准
董晓荣教授介绍,鳞癌是 NSCLC 的第二大组织类型;与靶向药物在腺癌治疗中占据举足轻重的地位不同的是,在过去二十年中,靶向药物在肺鳞癌治疗中的地位有限,其治疗仍以化疗为主。虽然 SQUIRE 研究显示 EGFR 单抗联合 GP 方案(吉西他滨+顺铂)相比化疗可以给晚期肺鳞癌患者带来生存获益,但是中位总生存期(mOS)也仅达到 11.5 个月 [3]。免疫治疗的到来为肺鳞癌治疗带来实现新突破的可能。
在 2019 年欧洲肿瘤内科学会亚洲会议(ESMO Asia)上,KEYNOTE-407 研究公布了中国人群研究结果,结果显示帕博利珠单抗联合化疗(紫杉醇+卡铂)组和化疗组(安慰剂+紫杉醇+卡铂)的 mOS 分别为 17.3 个月 vs 12.6 个月,联合治疗组较化疗组降低了 56% 的死亡风险;联合治疗组和化疗组中位无进展生存期(mPFS)分别为 8.3 个月 vs 4.2 个月,联合治疗组较化疗组降低了 68% 的疾病进展或死亡风险;此外,相比化疗组,联合治疗组的客观缓解率(ORR)提升了 36.8%(ORR:78.5% vs 41.7%)[4]。
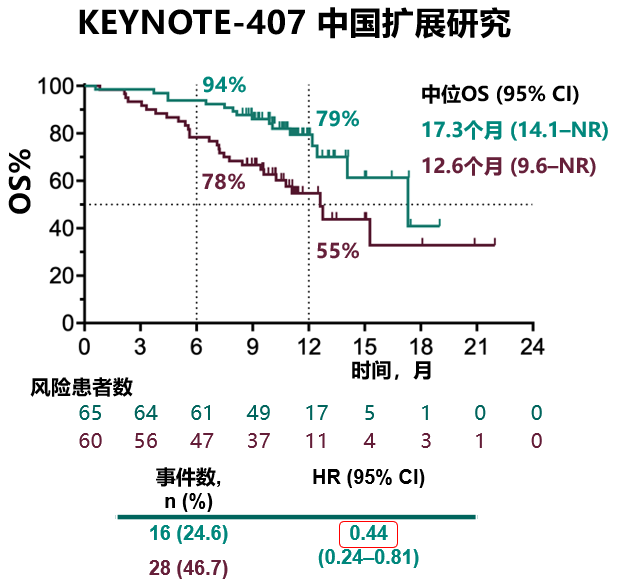
KEYNOTE-407 III 期临床研究中中国亚组 OS 数据结果显示帕博利珠单抗联合化疗一线治疗降低 56% 的死亡风险
KEYNOTE-407 全球研究结果显示,在所有的意向治疗人群中,帕博利珠单抗联合化疗组和化疗组的 mOS 分别为 17.1 个月 vs11.6 个月,联合治疗组较化疗降低了 29% 的死亡风险。两组 mPFS 分别为 8.0 个月 vs5.1 个月,联合治疗组降低了 43% 的疾病进展或死亡风险。此外,相比化疗组,联合治疗组的 ORR 提升了 24.1%(ORR:62.6% vs 38.4%)[5]。
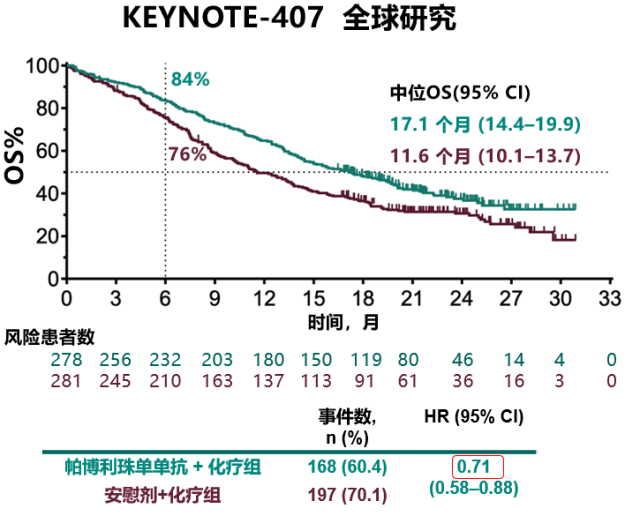
KEYNOTE-407 研究的 OS 数据结果显示帕博利珠单抗联合化疗一线治疗降低 29% 的死亡风险
由此可见,KEYNOTE-407 中国人群数据与全球数据保持一致:整体人群死亡风险降低 29%, 中国人群死亡风险降低 56%。对此董晓荣教授表示,中国晚期肺鳞癌患者似乎能从免疫一线联合治疗中得到生存获益,这可能与人种差异有关。一线免疫联合化疗给晚期肺鳞癌的治疗格局带来了重大突破,有望成为国内未来临床实践的新标准。
国内晚期 NSCLC 患者免疫一线治疗临床实践现状与美国存在一定差距
2019 年 3 月 28 日,帕博利珠单抗联合培美曲塞和铂类化疗一线治疗 EGFR 基因突变阴性和 ALK 阴性的转移性非鳞状 NSCLC 的适应证在国内获批(比美国仅晚了 7 个多月),此次获批是基于 KEYNOTE-189 研究结果,在中位随访 10.5 个月的时候,就已经观察到帕博利珠单抗联合化疗组带来的 OS 改善,与对照组相比降低 51% 的死亡风险 [6]。
在 2019 美国临床肿瘤学会年会(ASCO)上,KEYNOTE-189 研究更新了延长随访后的研究数据,在中位随访时间 18.7 个月后,帕博利珠单抗联合化疗组与化疗组的 mOS 分别为 22.0 vs 10.7 个月,mPFS 分别为 9.0 vs 4.9 个月 [7]。
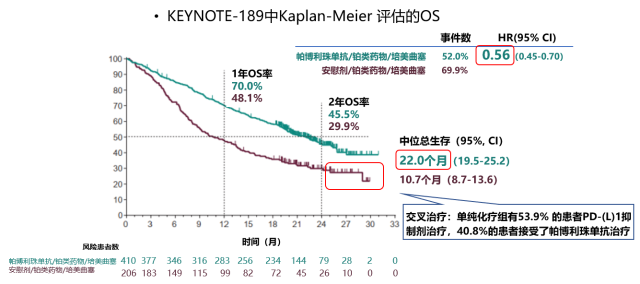
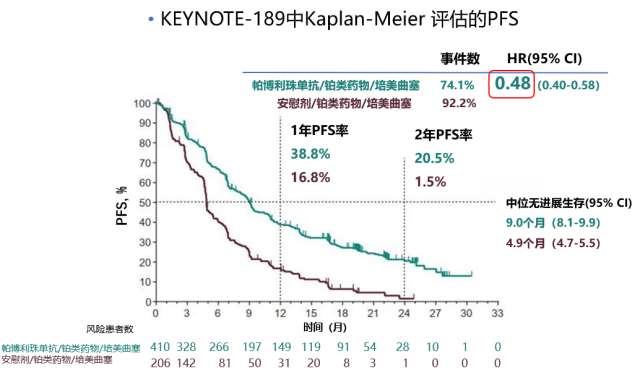
在 2019 年 ASCO 大会上公布的 KEYNOTE-189 中帕博利珠单抗联合化疗一线治疗非鳞 NSCLC 人群随访 18.7 个月的 OS 和 PFS 数据
基于 KEYNOTE-189 和 KEYNOTE-407 这两个研究的阳性结果,美国 FDA 分别于 2018 年 8 月和 10 月批准了帕博利珠单抗联合化疗一线治疗非鳞和鳞状晚期 NSCLC。 从此,免疫一线治疗迅速、并全面进驻驱动基因突变阴性的晚期 NSCLC 治疗。
在 2019 年,国内一线免疫治疗的发展情况如何呢?朱正飞教授表示,药物从获批到进入医保有一个过程。在免疫药物进入医保之前,一线免疫治疗使用比例与地域和经济差异相关,比如在北京、上海、广州等经济发达地区,一线使用免疫联合化疗的 NSCLC 患者比例相对较高。另外由于医疗水平不同,不同级别医院使用免疫治疗的比例也有存在一定差别。 因此,我国晚期 NSCLC 患者免疫一线治疗临床实践现状与美国相比还存在一定差距。未来需要多方努力,打破经济和医疗水平等因素制约,从而缩小与发达国家临床实践的差距,让更多患者获益于一线免疫治疗。
免疫治疗药物的选择及疗效判断方法
免疫药物的选择是临床医生在使用免疫治疗时面临的首要问题。朱正飞教授指出,不同的免疫药物在联合治疗临床研究中的结果除了与研究设计有关,也与药物本身有关。
首先,PD-1 单抗和 PD-L1 单抗就有很大区别,虽然作用于同一通路,但是 PD-1 存在于淋巴细胞上,而 PD-L1 存在于肿瘤细胞上,但由于 PD-L2 等因素的存在,阻断 PD-1 单抗和阻断 PD-L1 单抗产生的效果并不完全相同。另外 PD-1 单抗和 PD-L1 单抗的毒性反应也可能不同。
此外,不同的 PD-1 单抗之间也有很大差异,从药物结构到临床数据验证,毒性反应等等,这也证实了为何不同 PD-1 获得的适应证完全不同。在生产工艺和毒性反应上也存在差异。朱正飞教授表示,虽然目前国内已经有多个 PD-1 单抗和 PD-L1 单抗获批,但是临床决策应尽可能根据临床研究结果和药物获批适应证选择免疫治疗药物。
参考文献
[1] 中华人民共和国国家卫生健康委员会. 原发性肺癌诊疗规范(2018 年版)[J]. 肿瘤综合治疗电子杂志, 2019, 5(3): 100-120.
[2]Luis Paz-Ares, Alexander Luft, David Vicente, et al. Pembrolizumab plus Chemotherapy for Squamous Non–Small-Cell Lung Cancer[J].N Engl J Med 2018; 379:2040-2051.
[3]Thatcher N, Hirsch FR, Luft AV, et al. Necitumumab plus gemcitabine and cisplatin versus gemcitabine and cisplatin alone as first-line therapy in patients with stage IV squamous non-small-cell lung cancer (SQUIRE): an open-label, randomised, controlled phase 3 trial[J].Lancet Oncol. 2015 ;16(7):763-74.
[4]Cheng Y et al.,KEYNOTE-407 China Extension Study: Pembrolizumab Plus Chemotherapy in Chinese Patients with Metastatic Squamous NSCLC, Oral Presentation, ESMO-Asia, 2019
[5]Luis Paz-Ares et al., Pembrolizumab plus Chemotherapy in Metastatic Squamous NSCLC: Final Analysis and Progression After the Next Line of Therapy (PFS2)in KEYNOTE-407 ESMO, 2019
[6]Leena Gandhi, Delvys Rodríguez-Abreu, Shirish Gadgeel, et al. Pembrolizumab plus Chemotherapy in Metastatic Non–Small-Cell Lung Cancer[J]. N Engl J Med 2018; 378:2078-2092
[7]Gadgeel SM., et al. KEYNOTE-189: Updated OS and progression after the next line of therapy (PFS2) with pembrolizumab (pembro) plus chemo with pemetrexed and platinum vs placebo plus chemo for metastatic nonsquamous NSCLC." ASCO 2019 abstract 9013.
*本采访由默沙东支持
本资料仅代表个人观点,仅作学术交流之用,请勿分发或转发
03-2021-CN-LAM-00039