急性冠脉综合征(ACS)是一组在冠状动脉粥样硬化基础上,以斑块破裂、血栓、栓塞或血管痉挛为病理生理特点的急性心肌缺血事件的临床综合征。患者多以胸痛或胸部不适为首发症状,可导致心律失常、心力衰竭、甚至猝死,多在急诊科首诊,是急诊科常见疾病,也是急诊科的主要致死疾病之一。急诊科初诊过程中早期识别及正确处理与 ACS 患者的预后密切相关。
一. ACS 的诊断
1. ACS 诊断标准

2. ACS 的主要病理机制
ACS 的主要病理生理机制中,斑块破裂导致血栓形成占 60%~70%,斑块侵蚀导致血栓形成占 30%~40%。仅从斑块角度来评估血栓风险远远不够,急性血栓事件往往由多种因素共同交叉导致,下图所示。
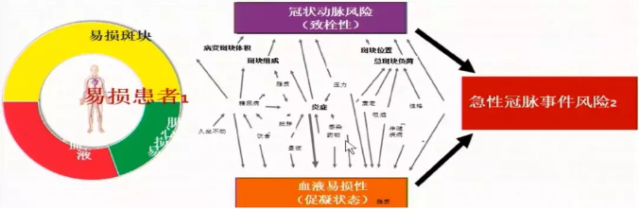
3. 鉴别 UA/NSTEMI
不稳定心绞痛(UA)患者的心肌损伤标记物不升高,非 ST 段抬高型心肌梗死(NSTEMI)患者的心肌标记物升高,可通过 hs-cTn 检测对 NSTE-ACS 患者进行诊断和鉴别诊断。
二. ACS 患者往往既是已损患者又是易损患者胸痛患者首次医疗接触(FMC)10 分钟内应尽快完成标准 12 导联或 18 导联心电图。结合症状及心电图进行疾病类型鉴别,即 ST 段抬高型心肌梗死(STEMI)或非 ST 段抬高型急性冠脉综合征(NSTE-ACS),并启动相应的治疗流程。
ACS 诊疗流程图。
1. 早期 GRACE 风险评估
2. 早期 TIMI 风险评估
3. CRUSADE 出血风险评估
该模型可以有效识别接受 ≥ 2 种和<2 种抗血小板药物、接受有创和保守治疗的出血风险。基于 CRUSADE 出血评分,将患者分为 5 级。CRUSADE 出血评分越高,患者的出血风险就越高。
三. ACS 抗栓治疗
血小板在 ACS 血栓形成过程中具有重要作用。ACS 急性期血小板呈爆发式激活,斑块破裂或侵蚀→急性血栓形成或栓塞→持续血栓激活,所以需尽早、充分干预。
(1)抗血小板治疗
1. NSTE-ACS 患者 PCI 术前预处理及抗血小板治疗推荐
对接受 PCI 治疗的 NSTE-ACS 患者,一经确认,应考虑使用替格瑞洛术前治疗。
2. STEMI 行 PCI 患者预处理及抗血小板治疗推荐
3. STEMI 患者 PCI 术中抗栓治疗推荐
(2)DAPT 策略
1. 接受药物治疗的 ACS 患者双联抗血小板治疗(DAPT)推荐
2. 不同诊断、不同治疗患者的 DAPT 方案
3. 拟行溶栓治疗的 STEMI 患者 DAPT 策略
拟行溶栓治疗的 STEMI 患者,年龄<75 岁者,P2Y12 受体抑制剂可选择替格瑞洛或氯吡格雷,替格瑞洛剂量方法同上;年龄 ≥ 75 岁者,P2Y12 受体抑制剂建议选择氯吡格雷,不使用负荷剂量,首剂 75 mg 口服,继予 75 mg/d 维持。
(3)口服 P2Y12 受体抑制剂的换药推荐
1. 急性期 P2Y12 受体抑制剂换药方法
2. 慢性期 P2Y12 受体抑制剂换药方法
(4)糖蛋白Ⅱb/Ⅲa 受体拮抗剂指南推荐
EARLY-ACS 研究,随机纳入 9492 例 NSTE-ACS 患者,DAPT-肝素治疗,随机分为两组,观察组早期采用依替巴肽治疗(造影前 12 小时使用),对照组采用延迟依替巴肽治疗(造影后即刻使用)。主要终点是 96 小时内死亡、心梗、需要血运重建的再发缺血事件或 PC 期间血栓并发症的复合终点。结果显示,造影前给予糖蛋白Ⅱb/Ⅲa 受体拮抗剂未降低缺血事件风险,但显著增加大出血风险,如下图所示。
(5)使用普通肝素与低分子肝素的指南建议
SYNERGY 研究显示,普通肝素与低分子肝素交叉使用可显著增加大出血风险。
(6)拟行 PCI 的 STEMI 患者的用药方案
(7)溶栓治疗
1. 拟接受溶栓治疗的 STEMI 患者
2. NSTE-ACS 患者 PCI 术中抗栓治疗推荐
(8)抗凝治疗
1. NSTE-ACS 患者的抗凝治疗
一项随机对照研究纳入 5239 例患者,其中 2153 例 PCI 术后接受抗凝治疗(比卢伐定或肝素)。研究显示,术后抗凝和不抗凝两组在死亡、心血管死亡、心梗、缺血导致血运重建、主要不良心血管事件、支架内血栓等均无统计学差异(P>0.05),而在主要出血方面,术后不抗凝组明显低于术后抗凝组(P<0.05),如下图所示。
STEMI 患者在直接 PCI 术后继续抗凝治疗未能显著减少主要缺血事件,但显著增加大出血风险。
2. NSTE-ACS 患者 PCI 术后继续肠外抗凝治疗对临床结局的影响
一项研究纳入 8197 例 NSTE-ACS 接受 PCI 治疗的患者,评估 NSTE-ACS 患者 PCI 术后继续肠外抗凝治疗对临床结局的影响。主要终点是院内全因死亡,主要安全性终点是院内主要出血(BARC 3~5 级)。结果显示,NSTE-ACS 患者 PCI 术后继续肠外抗凝治疗未能减少死亡和心梗,但显著增加主要出血风险,如下图所示。
肠外抗凝治疗对全因死亡、心梗、主要出血风险的影响在 GRACE 或 CRUSADE 评分不同的亚组患者间无显著差异。
3. ACS 患者 PCI 术后不建议常规抗凝治疗
· 增加缺血性风险的因素:高龄、存在 ACS、既往多发心肌梗死、广泛性冠状动脉疾病、糖尿病、慢性肾脏病(CKD)。
· 增加出血风险的因素:出血既往史、口服抗凝药、女性、高龄、低体重、CKD、糖尿病、贫血、长期类固醇或 NSAID 治疗。
4. 合并 CKD 患者的药物治疗
① 合并 CKD 患者抗血小板药物的剂量调整方案
② 合并 CKD 患者抗凝药物的剂量调整方案
③ 合并肾功能不全的 ACS 患者抗栓药物的用法及调整方案
④ 长期使用口服抗凝药的抗栓策略
四. ACS 患者院间转运策略
(1)STEMI 患者的转运策略
1. STEMI 患者的转运推荐
一项队列研究纳入 63 例发病 12 小时内行直接 PCI 的 STEMI 患者,使用 6.0T CMR 检测到微循环障碍和心肌内出血。研究显示,STEMI 患者在发病 4~6 小时内接受 PCI,其心肌内出血发生率最高,如下图所示。
STEMI 患者时间窗外行 PCI 应具备以下条件:有存活心肌、病情稳定、梗死区心肌完全恢复、心功能稳定、梗死相关血管(IRA)病变稳定、已无心脏破裂风险。
2. STEMI 患者延迟 PCI 何时做?做不做?
(2)NSTE-ACS 患者的转运策略
1. NSTE-ACS 应早期行侵入性诊断评估
· 药物治疗失败的患者,如难治性心绞痛、静息心绞痛或积极药物治疗但疗效有限;
· 非侵入性的运动试验提示有缺血的客观证据(心电图动态变化、心肌灌注缺损)的患者;
· 有提示极高危预后风险的临床指标(例如高 TIMI 或 GRACE 评分)的患者。
2. NSTE-ACS 患者有创治疗策略风险标准
3. NSTE-ACS 介入治疗时机
4. 不推荐早期行侵入性策略的情况
· 有严重并存疾病的患者(肝功能衰竭、肾功能衰竭、肺功能衰竭、癌症),不推荐早期侵入性治疗策略,因为此时血运重建和并存疾病的风险可能超过血运重建的获益;
· ACS 可能性较低的急性胸痛患者,如肌钙蛋白阴性,尤其是女性。
参考资料李拥军. 2019 中国急性冠状动脉综合征患者早期抗栓治疗及院间转运专家共识解读. 长城会 2019