关键词:慢性乙型肝炎;青少年;富马酸丙酚替诺福韦
一、病例介绍
患者男性,12 岁,学生,2016 年体检发现 HBsAg 阳性,当时肝功能正常,肝纤谱正常,乙型肝炎病毒分型为 B 型,肝脏弹力成像正常。3 年间,规律随访肝功能,于 2019 年 3 月随访 HBV-DNA 为 7.26×107IU/ml,HBsAg>25000 IU/ml,HBeAg 907.64 S/CO,HBcAb 8.17 S/CO,肝功能显示 ALT 176U/L、AST 86U/L,肾功能正常,肝纤谱显示 III 型前胶原 N 端肽升高为 51.56ng/ml。既往无手术史及外伤史,否认输血史,无嗜酒嗜烟。查体:生命体征平稳,神志清楚,皮肤、巩膜无黄染,未见蜘蛛痣,未见肝掌,心肺听诊无特殊异常,腹软,全服无压痛、反跳痛,肝肋下未触及,肝区无叩痛,移动性浊音阴性,双下肢无水肿。
二、临床诊治思维过程
患者青少年男性,诊断为慢性乙型病毒性肝炎,2019 年 3 月予以富马酸丙酚替诺福韦 25 mg qd 治疗,治疗一个月后,2019 年 4 月复查肝功能显示 ALT 33 U/L,AST 57 U/L,HBV-DNA 为 1.44×105 IU/ml,肾功能显示肌酐 58μmol/L(参考值范围:22-51μmol/L)。富马酸丙酚替诺福韦治疗一个月后,HBV-DNA 较前明显下降,肝功能也明显好转,提示富马酸丙酚替诺福韦治疗有效。患者服药前肾功能正常,既往无慢性肾病史,由于肌酐只是轻微升高,考虑肾前性原因所致,故暂不予以停药。2019 年 5 月(于当地中医院)复查肝功能显示 ALT 82.2 U/L,AST 54.2 U/L,HBV-DNA 为 1.5×103 IU/ml,肾功能显示肌酐 56μmol/L(参考值范围:57-97μmol/L),肌酐恢复正常。2019 年 6 月(于当地中医院)复查肝功能显示 ALT 77.3 U/L,AST 47.1 U/L,肾功能显示肌酐 59μmol/L(参考值范围:57-97μmol/L),肌酐恢复正常。患者肾功能自行恢复正常,同时,HBV-DNA 明显下降,肝功能也明显好转,故继续富马酸丙酚替诺福韦抗病毒治疗,并嘱患者规律随访肝肾功能、HBV-DNA 定量、乙肝两对半、肝纤谱、腹部彩超等。(相关指标见表 1)。
表 1 患者使用 TAF 后 ALT、肌酐、HBV DNA 的变化情况
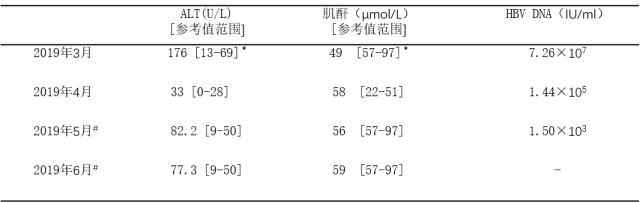
注:*表示急诊生化检验,#表示患者于当地医院复查。
三、治疗体会
富马酸丙酚替诺福韦(TAF)的有效成分为丙酚替诺福韦,其为替诺福韦的一种亚磷酰胺药物前体。丙酚替诺福韦进入肝细胞内,经过水解及磷酸化,形成药理学活性代谢产物二磷酸替诺福韦。二磷酸替诺福韦借助 HBV 逆转录酶整合嵌入病毒,从而抑制 HBV 复制 [1]。TAF 和富马酸替诺福韦酯(TDF)都是替诺福韦的药物前体,TAF 在血浆中更稳定,能够靶向 HBV 感染的肝细胞,提供更高水平的细胞内活性代谢产物二磷酸替诺福韦,因此能以更小的剂量给药,从而减少了血循环中的替诺福韦暴露,对肾功能及骨密度产生的不良反应更小 [2,3]。

既往研究大多基于年龄>18 岁的成年人,青少年慢性乙肝患者使用 TAF 出现的不良反应相关报道较少。TAF 的说明书上表明年龄不低于 12 岁,体重不低于 35 kg 的患者与成年人的使用相同。本例患者为 12 岁的青少年,既往无慢性肾病史,在使用 TAF 治疗过程中,出现了短暂的肌酐升高,eGFR 未见异常,随后肌酐自行恢复正常且维持正常,未出现肾功能的进行性恶化,表明 TAF 在年龄不低于 12 岁的青少年中使用是安全的。尽管如此,由于青少年慢性乙肝患者使用 TAF 的不良反应相关报道较少,因此,临床医生在对青少年患者使用 TAF 时也不可掉以轻心,仍应该在用药前及用药过程中,密切关注患者各方面的情况,警惕可能出现的不良反应。
据相关研究统计表明,我国慢乙肝患者呈现老龄化,合并高血压、糖尿病、代谢综合征等其它系统疾病的患者比例增加 [4],这些均为肾脏损害的危险因素,同时,HBV 病毒本身也会对肾脏功能造成影响,因此,对肾功能影响较小的抗病毒药物是我国对治疗慢乙肝患者的一大诉求。恩替卡韦、替诺福韦酯、阿德福韦酯等核苷酸类似物均可造成肾脏功能损害。TAF 于 2019 年 1 月在中国正式上市,以往研究表明,TAF 不管是用于抗 HIV 病毒还是用于抗 HBV 病毒,相对于 TDF, 其抗病毒的效果与 TDF 相当,但是其对肾功能和骨密度的影响明显小于 TDF,血清肌酐升高、肾小球滤过率降低、近端肾小球功能障碍等肾功能损害的发生率均明显低于 TDF[5,6,7]。对于有潜在肾脏功能受损风险以及肾脏功能已经受损的慢乙肝患者,应该优先选择 TAF 作为抗病毒治疗的药物。
TAF 作为一种新型抗病毒药物应用于慢乙肝患者的治疗中,其病毒学应答率与 TDF 相当,但其安全性优于 TDF,此为慢乙肝患者的一大福音。临床医生在使用 TAF 的过程中,仍不可忽略 TAF 可能存在的不良反应,需密切关注患者的治疗反应,将 TAF 这件利器的作用发挥至最好。

参考文献
[1] Milburn J, Jones R, Levy JB. Renal effects of novel antiretroviral drugs. Nephrology Dialysis Transplantation, 2016:gfw064.
[2] Robbins BL, Srinivas R, Kim C, et al. Anti-Human Immunodeficiency Virus Activity and Cellular Metabolism of a Potential Prodrug of the Acyclic Nucleoside Phosphonate 9-R-(2-Phosphonomethoxypropyl) adenine (PMPA), Bis (isopropyloxymethylcarbonyl) PMPA. Antimicrobial Agents & Chemotherapy, 1998, 42(3):612.
[3] Liu Y, Mitchell B, Dinh P, et al. Antiviral activity of tenofovir alafenamide against drug-resistant HBV isolates in vitro. Hepatology (Baltimore), 2016; 64:1194A.
[4] 杨益大,陈文东,韩英 等 中国城镇慢性乙型肝炎患者老龄化和共患病增加:基于 2013-2016 年医保数据的回顾性分析. 第十届全国疑难及重症肝病大会 2019.
[5] Chan HLY, Fung S, Seto WK, et al. Tenofovir alafenamide versus tenofovir disoproxil fumarate for the treatment of HBeAg-positive chronic hepatitis B virus infection: a randomised, double-blind, phase 3, non-inferiority trial. The Lancet Gastroenterology & Hepatology, 2016:S2468125316300243.
[6] Buti M, Gane E, Seto WK, et al. Tenofovir alafenamide versus tenofovir disoproxil fumarate for the treatment of patients with HBeAg-negative chronic hepatitis B virus infection: a randomised, double-blind, phase 3, non-inferiority trial. The Lancet Gastroenterology & Hepatology, 2016:S2468125316301078.
[7] Gupta SK , Post FA , Arribas JR, et al. Renal safety of tenofovir alafenamide vs tenofovir disoproxil fumarate: A pooled analysis of 26 clinical trials. AIDS, 2019, publish ahead of print.